L'età approvata per l'uso della clonidina transdermica è di 18 anni e oltre.Non è esplicitamente approvata per i minori di 18 anni.Il Cerotto transdermico alla clonidina è stato approvato dalla FDA nel 1984 per il trattamento dell'ipertensione da lieve a moderata, da solo o con un diuretico, e funziona come un agente ipotensivo alfa-agonista ad azione centrale.
Punti chiave spiegati:
-
Limitazione dell'età approvata dalla FDA
- La clonidina transdermica non è non è approvata per i pazienti di età inferiore ai 18 anni .Questa restrizione è ripetuta in più riferimenti, sottolineando la sua importanza nell'uso clinico.
- Il cerotto è indicato specificamente per gli adulti (dai 18 anni in su), probabilmente a causa dell'insufficienza dei dati di sicurezza/efficacia nelle popolazioni pediatriche o dei rischi potenziali propri dei pazienti più giovani.
-
Uso medico primario
- Approvato per il trattamento di ipertensione da lieve a moderata (pressione alta), in monoterapia o in combinazione con un diuretico.
- Il suo meccanismo consiste nell'agire come alfa-agonista ad azione centrale che riduce l'attività del sistema nervoso simpatico per abbassare la pressione sanguigna.
-
Contesto normativo
- La FDA ha approvato la formulazione transdermica nel 1984 a testimonianza del suo ruolo di lunga data nella gestione dell'ipertensione.
- La limitazione dell'età è rimasta costante dall'approvazione, il che suggerisce che non ci sono prove successive a sostegno dell'uso pediatrico.
-
Considerazioni cliniche per gli acquirenti
- Gli operatori sanitari che acquistano il cerotto devono verificare l'età del paziente per evitare un uso off-label nei bambini.
- La restrizione implica che per i pazienti pediatrici potrebbero essere necessarie terapie antipertensive alternative.
Questa chiarezza garantisce la conformità alle linee guida di prescrizione e la sicurezza del paziente.Per le popolazioni adulte, il cerotto offre un'opzione non orale per il controllo della pressione arteriosa, un dettaglio prezioso per i responsabili della formulazione.
Tabella riassuntiva:
| Aspetto chiave | Dettagli |
|---|---|
| Fascia d'età approvata | 18 anni e oltre (non per uso pediatrico) |
| Uso primario | Trattamento dell'ipertensione lieve-moderata |
| Meccanismo d'azione | Alfa-agonista ad azione centrale per abbassare la pressione arteriosa |
| Anno di approvazione della FDA | 1984 |
| Considerazioni cliniche | Verificare l'età del paziente; per i pazienti sotto i 18 anni sono necessarie terapie alternative |
Avete bisogno di soluzioni transdermiche affidabili per la gestione dell'ipertensione negli adulti?
Enokon è specializzata nella produzione di cerotti transdermici di alta qualità, comprese le formulazioni di clonidina, per i distributori di prodotti sanitari e i marchi farmaceutici.La nostra esperienza garantisce la conformità alle linee guida della FDA e la perfetta integrazione nella vostra linea di prodotti.
Contattateci oggi stesso per discutere di ricerca e sviluppo personalizzati, ordini di grandi quantità o supporto normativo: miglioriamo insieme la cura dei pazienti.
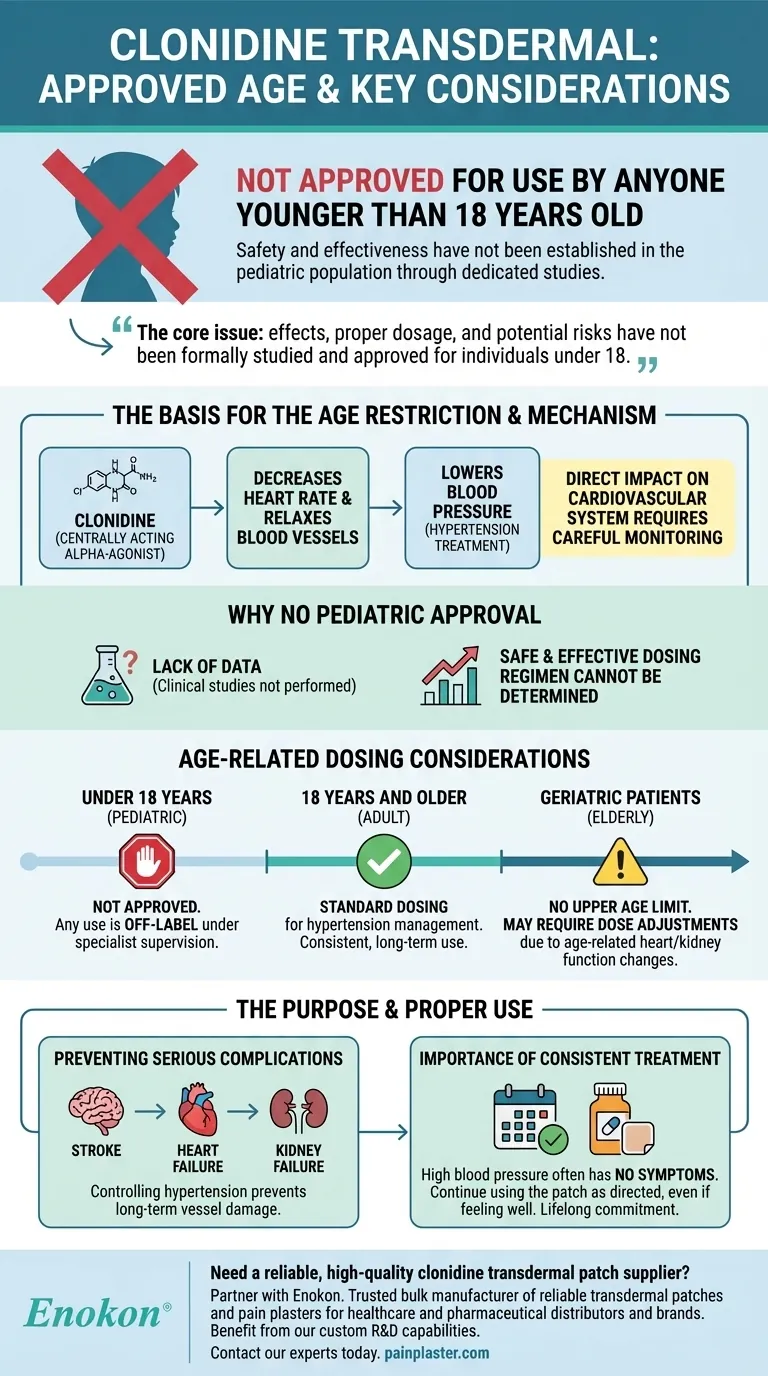
Guida Visiva
Prodotti correlati
- Cerotti antidolorifici al calore dell'infrarosso lontano Cerotti transdermici
- Toppa in silicone per cicatrici Toppa transdermica per farmaci
- Cerotto antidolorifico di medicina al mentolo Icy Hot
- Cerotto antidolorifico in gel al mentolo
- Cerotto antidolorifico all'artemisia per i dolori al collo
Domande frequenti
- Che ruolo svolgono i cerotti transdermici nel migliorare le lesioni cutanee? Scopri come la stabilizzazione previene le piaghe da decubito
- Quali vantaggi clinici offrono i cerotti transdermici ai pazienti anziani?Ottimizzare l'assistenza geriatrica con facilità
- Quale ruolo svolge un essiccatore nell'analisi del contenuto di umidità dei cerotti transdermici? Garantire stabilità e sicurezza
- Quali sono i principali vantaggi dell'uso dei cerotti transdermici?Scoprite i vantaggi di una somministrazione di farmaci senza dolore
- Quali fattori influenzano l'efficacia dei cerotti transdermici?Considerazioni chiave per una somministrazione ottimale del farmaco











